
II
Olimpíada Norte - Nordeste de QuímicaExame aplicado em 26.10.96
Problema
1A tabela abaixo representa os quatro primeiros períodos da classificação periódica. Baseado na posição dos elementos mencionados nesta tabela, determine:

a. O número atômico do elemento Fe?
b. Considere o elemento Cr. No estado fundamental, qual a configuração eletrônica do íon estável que esse elemento pode formar?
c. A qual período e família pertence o elemento manganês?
d. O que existe de comum na estrutura eletrônica dos átomos dos elementos C, N, O, F e Ne no estado fundamental?
e. Qual o conjunto de números quânticos do elétron de valência do átomo de sódio?
f. Como varia a eletronegatividade dos elementos situados no 3o período?
g. Qual a fórmula provável de um composto formado entre os elementos magnésio e cloro?
h. Qual á a forma geométrica da molécula NH3?
i. O que ocorre quando CaCl2(s) é dissolvido em água e quais tipos de ligação são desfeitas neste processo?
j. A partir da posição dos elementos de transição mencionados na tabela, indique para cada elemento:
Problema
2As propriedades ácidas do suco de limão são atribuídas à presença do ácido cítrico. Assim, a reação entre o componente ácido do suco de limão e o hidróxido de sódio pode ser quimicamente representado pela seguinte equação balanceada:
H2C-COOH |
H2C-COO- Na+ |
||||
½ |
½ |
||||
HOC-COOH |
+ 3 NaOH (aq) |
« |
HOC-COO- Na+ + 3 H2O |
||
½ |
½ |
||||
H2C-COOH (aq) |
H2C-COO- Na+ (aq) |
||||
Um estudante, ao titular suco de limão, anotou os seguintes dados:
ALÍQUOTA DO SUCO DE LIMÃO |
ÁGUA DESTILADA |
INDICADOR, FENOLFTALEÍNA |
VOLUME de NaOH 0,10 mol/L, GASTO NA TITULAÇÃO |
3 mL |
30 mL |
3 gotas |
6,0 mL |
Baseado na equação e nos dados acima, responda:
a. Classifique a reação que ocorre nesta titulação.
b. Que massa de NaOH é necessária na preparação de 500 mL da solução utilizada na titulação?
c. Por que adicionam cerca de 30 mL de água destilada antes da titulação?
d. Para que foi usada a fenolftaleína nesta análise?
e. Considerando a quantidade de solução gasta na titulação, calcule o número de mols de NaOH presente nesse volume.
f. Qual o número de mols de ácido cítrico presente nos 3 mL do suco de limão?
g. Qual a concentração, em mol/L e em g/L, do ácido cítrico no suco de limão?
h. Se um indivíduo toma 50 mL desse suco de limão, quantos gramas de ácido cítrico foram ingeridos?
i. O que ocorre quando se expreme limão sobre uma porção de carbonato ácido de sódio?
j. Que outra solução poderia ser utilizada em substituição a de NaOH?
Dados: M(H) = 1 g/mol; M(C) = 12 g/mol; M(O) = 16 g/mol; M(Na) = 23 g/mol.
Problema
3Uma célula eletroquímica é constituída por:
Eletrodo A - fio de platina que mergulha numa solução que contém íons Fe+3 e Fe+2 , ambos com concentração 1 mol/L.
Eletrodo B - vareta de tálio mergulhada numa solução 1 mol/L de Tl +1 .
Sabendo que os potenciais-padrão referentes às semi-reações:
Tl +1 + e- ® Tl
Fe+3 + e- ® Fe+2
são, respectivamente, - 0,34 V e + 0,77 V, faça o que se pede:
a. Mostre as semi-reações que ocorrem no cátodo e no ânodo.
b. Escreva a equação da reação que ocorre na célula.
c. Calcule o potencial da célula.
d. O que ocorrerá com o potencial da célula se diminuirmos a concentração de Tl+1 no eletrodo B?
Problema
4Traduza, sob forma de equações, as reações químicas descritas a seguir. Para cada caso, informe o tipo de reação ocorrida, escolhendo dentre as possibilidades enumeradas a seguir. Para cada resposta dada, justifique a escolha feita.
a. Nos motores de explosão que consomem álcool combustível, estando mal regulados, o álcool etílico sob a ação do oxigênio atmosférico transforma-se em acetaldeído, que é eliminado pelo escapamento juntamente com a água.
b. O acetato de ciclo-hexila é decomposto pelo calor quando submetido a altas temperaturas dando como produtos o ciclo-hexeno e o ácido acético.
c. O 2-buteno reage com o ácido sulfúrico a frio dando como produto o sulfato ácido de sec-butila.
d. O benzeno reage com o bromo em presença do tribrometo de ferro funcionando como catalisador. O produto desta reação é uma mistura de brometo de fenila e brometo de hidrogênio.
Problema
5Na matéria, os átomos estão muito próximos entre si e existem forças que os mantém juntos. Estas forças se chamam "ligações químicas".
1. Quais tipos de ligações são encontrados na substância NaHSO4 ?
2. a) Escreva uma estrutura de Lewis para a molécula NO2.
b) É possível emparelhar todos os elétrons desta espécie?
c) O NO2 é capaz de dimerizar para dar N2O4. Escreva uma estrutura de Lewis razoável para a molécula N2O4.
3. Dada a molécula do álcool etílico,
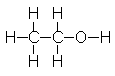
sabendo-se que a energia total das ligações é igual a 173 kcal/mol, determine a energia necessária para quebrar a ligação C - O considerando que:
H - C = 99 kcal/mol
H - O = 111 kcal/mol
C - C = 83 kcal/mol
4. Quais formas estruturais apresentam as espécies químicas: XeF4, BrF3 e I3-.
Números atômicos: H = 1; N = 7; C = 6; O = 8; Na = 11; S = 16; Br = 35; I = 53 e Xe = 54.
Números atômicos: H = 1; N = 7; C = 6; O = 8; Na = 11; S = 16; Br = 35; I = 53 e Xe = 54.