VII O
limpíada Norte - Nordeste de QuímicaExame aplicado em 26.05.2001
QUESTÃO 1
Escreva a nomenclatura ou a fórmula, conforme o caso, das
espécies químicas abaixo, cite uma aplicação e a função a que pertence cada uma
delas:
a) HCl;b)
NaOH; c) CaO;d) NH4OH;
e) H2O2; f) CH3COOH;
h) bicarbonato
de sódio ; i) sílica;
j) gás
carbônico.
QUESTÃO 2
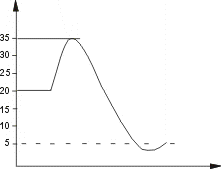
Dado o gráfico abaixo, que representa a energia, em Kcal/mol,
posta em jogo no decorrer de uma reação química:

a)Indique a
grandeza que deve ser representada no eixo dos "x";
b)Indique a
grandeza que deve ser representada no eixo dos "y";
c)Classifique a
reação, segundo a variação de energia ocorrida no processo;
d)Indique o
efeito da adição de um catalisador, no perfil do gráfico;
e)Calcule a
energia de ativação da reação "direta";
f)Calcule a
variação de entalpia (DH) nesta reação.
QUESTÃO 3
I) Explique por que :
a)O íon Li+
é menor que o íon Rb+, mas uma solução de RbCl apresenta maior
condutividade elétrica que outra de LiCl;
b)O ângulo HNH
na amônia se aproxima mais de um ângulo tetraédrico, enquanto o ângulo HPH na fosfina
está mais próximo de 90º.
II) Identifique e descreva as características dos tipos de
ligações químicas presentes nos materiais abaixo:
c) água líquida;d)hidrogênio gasoso;e) fragmento metálico.
QUESTÃO 4
I) Compare um gás e um líquido, no que se refere às seguintes
propriedades:
a) Densidade;b)
Compressibilidade;
c) Capacidade de se misturar com outras
substâncias, na mesma fase, e formar misturas homogêneas.
II) Uma
amostra de 8,04g de uma mistura de carbonato de cálcio e carbonato de magnésio foi
tratada com ácido clorídrico em excesso. A reação produziu 2,26 L de dióxido de
carbono gasoso, a 23 °C e 735 torr:
d)Dê as
equações químicas das reações entre o ácido clorídrico e cada um dos componentes da
mistura;
e)Calcule a
massa de dióxido de carbono formado nesta reação;
f)Admitindo que
as reações ocorrem completamente, calcule a porcentagem em massa de carbonato de
magnésio na mistura inicial.
QUESTÃO 5
I) Que são propriedades coligativas ? Cite e comente 3 (três)
exemplos.
II) A 35 °C,a pressão de
vapor da acetona é 360 torr e a do clorofórmio é 300 torr. A acetona e o clorofórmio
podem formar ligações de hidrogênio fracas, da seguinte forma:
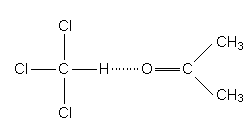
A pressão de
vapor de uma solução equimolar de acetona e clorofórmio é de 250 torr, a 35 °C:
a)Qual seria a
pressão de vapor desta solução se o comportamento fosse ideal ?
b)A que se deve
esse afastamento da idealidade ?Explique.
c)Com base no
comportamento da solução, diga, se o processo de misturar acetona com clorofórmio é um
processo exotérmico ou endotérmico?
Justifique.
O
geraniol é um terpeno presente no óleo de rosas:
I.Ao ser
submetido à reação de adição com Br2, forma um tetra-haleto;
II.Por
hidrogenação catalítica, ele produz um álcool de fórmula C10H22O;
III.Este álcool,
ao ser oxidado, leva à formação de um aldeído ou ácido carboxílico;
IV.Por
ozonólise, o geraniol se fragmenta formando os seguintes produtos:

a)Escreva as
equações químicas correspondentes a cada um dos ítens acima;
b)Proponha duas
estruturas possíveis para o geraniol;
c)Considerando
que o geraniol é constituído de unidades isoprênicas (2-metil-buta-2-eno), qual seria
sua verdadeira estrutura ?
d)Escreva o
nome sistemático para o geraniol e para os produtos de sua ozonólise.
Dados
(valores aproximados):
VOLTA
a menu principal