Olimpíada
Brasileira de Química - 2002
Fase
VI (final)
Questão
1
Boa
parte das propriedades dos metais depende da forma como seus átomos
encontram-se arranjados no espaço. A maioria dos metais comuns
apresenta arranjos atômicos cúbicos. Os sistemas de arranjos cúbicos
podem ser classificados em três diferentes tipos de repetição: cúbico
simples, o qual não é observado nos metais devido o baixo
empacotamento atômico; cúbico de corpo centrado, observado no crômio
metálico, por exemplo, e cúbico de faces centradas, observado, por
exemplo, no cobre metálico.
Uma
maneira de se calcular o espaço ocupado em cada célula unitária é
através do fator de empacotamento (FE), que pode ser obtido dividindo
o volume dos átomos da célula pelo volume da célula unitária.
a)
Sabendo disso, calcule o FE no cobre metálico, raio atômico 1,278 Å.
Compare esse valor com o FE do crômio metálico, cujo lado da face da
célula unitária apresenta um comprimento de 2,887 Å.
As
referidas estruturas cristalinas podem ser determinadas através de análise
por raio X. Quando um feixe de raios X é dirigido através de um
material cristalino, esses raios são difratados pelos planos dos átomos
do cristal. O ângulo de difração depende do comprimento de onda dos
raios X e das distâncias entre planos adjacentes. Estas distâncias
entre planos adjacentes correspondem aos espaçamentos de repetição
dos átomos em uma determinada direção. Os planos podem ser traçados
tendo-se como base os eixos x, y, z.
b)
Tendo lembrado disso, determine o raio atômico
do níquel, que possui estrutura cúbica de faces centradas, sabendo
que para se determinar o espaçamento entre os planos 200 no níquel,
usam-se raios X de comprimento de onda 0,58 Å e que o ângulo de
reflexão é 9,5 °.
Uma
determinada substância sofre decomposição segundo uma cinética de
primeira ordem, e sua dependência em relação à temperatura segue
uma lei empiríca chamada de equação de Arrhenius. Os tempos de
meia-vida determinados a 95ºC e 85ºC foram 15,4 minutos e 57,8
minutos, respectivamente.
A
partir destes dados:
a)
Calcule a energia de ativação e, supondo que esta permaneça
constante, independente da temperatura, estime o tempo de meia-vida a
25 ºC.
b)
Estime também a energia de ativação por meio de um gráfico
do logarítmo natural da constante de velocidade versus o
inverso da temperatura (em Kelvin).
Dados: Equação de Arrhenius:
R
= 8,314 J.K-1.mol-1
O
lantânio presente em 5,00 g de monazita foi convenientemente extraído
na forma de La3+
e concentrado em 100 mL de solução. Após
precipitação quantitativa do metal na forma de oxalato, La2(C2O4)3
,
o sal foi filtrado, lavado e redissolvido em quantidade adequada (~20
mL) de ácido sulfúrico 1,00 mol/L em erlenmeyer de 125 mL. Na titulação
desta solução com solução de KMnO4
0,0064 mol/L, foram gastos 36,1 mL.
Determine:
a)
A concentração de La3+
na solução inicial
b)
O teor de lantânio na monazita
Dados:
Massas
atômicas (aproximadas), g/mol:
La = 138,9
Mn = 54,9
K = 39,0
O =
16,0
C = 12,0
S = 32,0
O
íon Fe(III) pode formar complexos com as geometrias tetraédrica e
octaédrica. Entretanto, a maioria dos complexos de Fe(III) apresenta
geometria octaédrica e são complexos de spin baixo.
O
íon Co(III) forma complexos apenas octaédricos e, 99% destes, são
de spin baixo. Já o íon Co(II) pode formar complexos tetraédricos e
octaédricos de spin alto.
De acordo com as informações acima e
baseado na Teoria do Campo Cristalino (TCC), explique essa diferença
de comportamento entre esses íons.
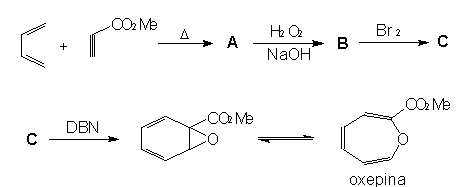
A oxepina pode ser
preparada no laboratório, não por oxidação direta do benzeno, mas,
através da seqüência de reações químicas apresentadas abaixo.
Complete
esta seqüência, indicando as estruturas, com especificação da
estereoquímica, quando for o caso, dos intermediários A, B e C.

DBN =
1,5-diaza-biciclo[4.3.0]nona-5-eno
Uma substância X que dá teste positivo com FeCl3,
mostra no seu espectro de massa o pico do íon molecular situado a 194
unidades de massa. Sua hidrólise catalisada por ácido fornece a
substância Y que é solúvel em solução de NaHCO3
a 10%. O espectro de RMN 1H
de X, obtido em CD3OD
a 500 MHz, apresenta os seguintes sinais:
d (ppm)
Multiplicidade e J (Hz)
Integração
3,75
s
3,12
6,30
d, J=15
1,20
6,75
d, J=8
1,03
6,94
dd, J=2 e 8
1,03
7,03
d, J=2
1,02
7,56
d, J=15
1,00
s = singlete; d = dublete; dd = dublete de
dublete.
O
espectro de RMN 13C
normal (desacoplado) de X apresenta dez sinais, o DEPT 135 seis sinais
e o DEPT 90 cinco sinais, conforme especificado:
52,1
positivo
não aparece
114,9
positivo
positivo
115,3
positivo
positivo
116,6
positivo
positivo
123,1
positivo
positivo
127,8
não aparece
não aparece
146,9
positivo
positivo
147,1
não aparece
não aparece
149,7
não aparece
não aparece
169,9
não aparece
não aparece
Com
base nestas informações, responda:
a)
Qual é a fórmula molecular de X?
b)
Quais as estruturas das substâncias X e Y?
c)
Que outra substância, além de Y, é formada na hidrólise
de X?
d)
Qual(is) do(s) sinal(is) do espectro de RMN 1H
de X não aparece no espectro de Y?
Dados:
Alguns
valores de deslocamentos químicos de 1H
H
aromático:
6 - 9 ppm;
H
olefínico:
4,2 - 7,6 ppm;
H
de ácido carboxílico:
10 - 13 ppm;
CH3-O-:
3,3 - 3,8 ppm;
RCH2-O-:
3,5 - 4,4 ppm:
R2CH-O-:
3,8 - 5,2 ppm;
R2C=CH-CO:
5,8 - 6,7 ppm;
RCH=C-CO: :;
6,5 - 7,8 ppm.
Alguns
valores de deslocamentos químicos de 13C
C
de
carbonila:
156 - 220 ppm;
C
aromático:
100 - 165 ppm;
C
olefínico:
110 - 150 ppm: